- CDC studija o sigurnosnom praćenju dodatne doze cjepiva protiv COVID-19
- Ono što je već poznato o the potiskivač?
- Među 306 sudionika kliničkog ispitivanja Pfizer-BioNTech, nuspojave nakon doze 3 bile su slične onima nakon doze 2.
Što se dodaje ovim izvještajem na snimci broj 3 koju je CDC objavio danas?
Tijekom 12. kolovoza-19. rujna 2021., među 12,591 v-sigurnih podnositelja registracije koji su završili anketu o zdravstvenoj prijavi nakon sve 3 doze cjepiva protiv mRNA COVID-19, 79.4% odnosno 74.1% prijavilo je lokalne, odnosno sistemske reakcije, nakon treća doza; 77.6% i 76.5% prijavilo je lokalne ili sustavne reakcije nakon druge doze.
Koje su implikacije za javnu zdravstvenu praksu?
Dobrovoljni izvještaji za v-safe nisu pronašli neočekivane obrasce nuspojava nakon dodatne doze cjepiva protiv COVID-19. CDC će nastaviti pratiti sigurnost cjepiva, uključujući dodatne doze COVID-19.
Dana 12. kolovoza 2021. Uprava za hranu i lijekove (FDA) izmijenila je Odobrenja za hitnu uporabu (EUA) za cjepiva Pfizer-BioNTech i Moderna COVID-19 kako bi odobrila primjenu dodatne doze nakon završetka serije primarnih cijepljenja osobama koje imaju pravo na umjerena do teška stanja s oslabljenim imunitetom (1,2). 22. rujna 2021. godine FDA je odobrila dodatnu dozu cjepiva Pfizer-BioNTech ≥6 mjeseci nakon završetka primarne serije među osobama u dobi od ≥65 godina, s visokim rizikom od ozbiljnog COVID-19 ili čija ih profesionalna ili institucionalna izloženost stavlja na visok rizik od COVID-19 (1). Rezultati kliničkog ispitivanja faze 3 koje je proveo Pfizer-BioNTech, a koje je obuhvatilo 306 osoba u dobi od 18 do 55 godina, pokazali su da su nuspojave nakon primanja treće doze primijenjene 5-8 mjeseci nakon završetka 2-dozne serije cijepljenja primarnom mRNA slične oni prijavljeni nakon primanja doze 2; ove nuspojave uključivale su blago do umjereno mjesto ubrizgavanja i sustavne reakcije (3). CDC je razvio v-safe, dobrovoljni sustav sigurnosnog nadzora temeljen na pametnim telefonima, koji pruža informacije o nuspojavama nakon cijepljenja protiv COVID-19.
Slučajno s odobrenjem dodatne doze za osobe s imunokompromitirajućim stanjima, platforma v-safe ažurirana je kako bi podnositeljima registracije omogućila unos podataka o dodatnim dozama primljenog cjepiva protiv COVID-19. Tijekom 12. kolovoza-19. rujna 2021. ukupno je 22,191 podnositelja registracije v-safe prijavilo primanje dodatne doze cjepiva protiv COVID-19. Većina (97.6%) izvijestila je o primarnoj seriji cijepljenja s 2 doze mRNA, nakon čega je uslijedila treća doza istog cjepiva. Među onima koji su ispunili zdravstveni pregled za sve 3 doze (12,591; 58.1%), 79.4% i 74.1% prijavilo je lokalne ili sustavne reakcije, nakon doze 3, u usporedbi sa 77.6% i 76.5% koje su prijavile lokalne ili sistemske reakcije, nakon doze 2. Ovi početni nalazi ukazuju na to da nema neočekivanih obrazaca nuspojava nakon dodatne doze cjepiva protiv COVID-19; većina ovih nuspojava bila je blaga ili umjerena. CDC će nastaviti pratiti sigurnost cjepiva, uključujući sigurnost dodatnih doza cjepiva protiv COVID-19, te pružati podatke za usmjeravanje preporuka cjepiva i zaštitu javnog zdravlja.
V-safe je dobrovoljni američki sustav sigurnosnog nadzora temeljen na pametnim telefonima; cijepljene osobe koje ispunjavaju uvjete za dobivanje odobrenog ili licenciranog cjepiva mogu se registrirati u v-safe. Platforma v-safe omogućuje postojećim podnositeljima registracije da prijave primanje dodatne doze cjepiva protiv COVID-19, a novim podnositeljima registracije unos podataka o svim primljenim dozama cjepiva protiv COVID-19. Ispitivanja o zdravlju V-zdravlja šalju se tijekom dana 0–7 nakon svake doze cjepiva i uključuju pitanja o lokalnom mjestu ubrizgavanja i sustavnim reakcijama i utjecajima na zdravlje.* Ankete se šalju za najnoviju unesenu dozu.† Članovi osoblja iz Sustava izvješćivanja o neželjenim događajima cjepiva (VAERS) kontaktiraju podnositelje registracija koji ukazuju na to da je nakon cijepljenja zatražena liječnička pomoć te potiču ili olakšavaju dovršavanje izvješća o VAERS -u, ako je navedeno.§
Među v-sigurnim podnositeljima registracije koji su prijavili primanje dodatne doze cjepiva protiv COVID-19 tijekom 12. kolovoza-19. rujna 2021. godine, demografski podaci, lokalne i sustavne reakcije i utjecaji na zdravlje prijavljeni tijekom dana 0–7 opisani su obrascem cijepljenja (tj. , proizvođač cjepiva primljenog za svaku dozu). Osobe koje su prijavile da su primile primarnu seriju od različitih proizvođača ili proizvođača koje su bile nepoznate ili nedostupne u Sjedinjenim Državama, ili 2 doze cjepiva nakon primanja Janssenovog (Johnson & Johnson) cjepiva s jednom dozom (150) isključene su iz analize nuspojava nakon primanja dodatne doze.
Vrijeme koje je proteklo od završetka primarne serije cijepljenja do primanja dodatne doze opisano je obrascem cijepljenja. Profili neželjenih događaja nakon doza 2 i 3 uspoređeni su za podnositelje registracija koji su primili cjepivo protiv mRNA od istog proizvođača za sve 3 doze.¶ Za provođenje svih analiza korišten je softver SAS (verzija 9.4; SAS institut). CDC je pregledao ove nadzorne aktivnosti i proveo ih u skladu s važećim saveznim zakonom i politikom CDC -a. **
Tijekom 12. kolovoza-19. rujna 2021. ukupno je 22,191 podnositelja registracije v-safe prijavilo primanje dodatne doze cjepiva protiv COVID-19 nakon završetka primarne serije (Tablica 1). Među njima je 14,048 (63.3%) žena, a otprilike 30% je bilo u dobi od 18–49, 50–64 i 65–74 godina.
Većina podnositelja registracije (21,662; 97.6%) izvijestila je da je primila treću dozu od istog proizvođača kao i njihova serija primarnih mRNA cjepiva, uključujući 98.6% primatelja Moderne i 98.2% primatelja Pfizer-BioNTech-a. Nekoliko podnositelja registracije (341; 1.5%) prijavilo je primarnu seriju cjepiva protiv mRNA, nakon čega je uslijedila dodatna doza cjepiva protiv mRNA drugog proizvođača, doza Janssenovog cjepiva nakon primitka serije primarnih cijepljenja protiv mRNA (10; 0.05%) ili dodatna dozu cjepiva protiv COVID-19 bilo kojeg proizvođača nakon cjepiva Janssen (178; 0.8%).
Među 22,191 v-sigurnih podnositelja registracije, srednji interval od završetka primarne serije cijepljenja protiv COVID-19 do primanja dodatne doze bio je 182 dana (interkvartilni raspon [IQR] = 160–202 dana) (Tablica 2). Među onima koji su primili 2 doze Janssenovog cjepiva, srednji interval između doza bio je kraći (84 dana; IQR = 16-136 dana).
Lokalne (16,615; 74.9%) i sustavne (15,503; 69.9%) reakcije često su prijavljivane tijekom tjedna nakon dodatne doze cjepiva protiv COVID-19, najčešće dan nakon cijepljenja. Često prijavljene reakcije bile su bol na mjestu ubrizgavanja (15,761; 71.0%), umor (12,429; 56.0%) i glavobolja (9,636; 43.4%).
Među 22,191 primatelja dodatne doze, ukupno 7,067 (31.8%) prijavilo je utjecaje na zdravlje, a otprilike 28.3% (6,287) je izjavilo da ne može obavljati normalne dnevne aktivnosti, najčešće dan nakon cijepljenja. Medicinsku skrb zatražio je 401 (1.8%) podnositelja zahtjeva, a trinaest (0.1%) je hospitalizirano. Razlozi za dobivanje medicinske skrbi ili hospitalizacije nisu identificirani u anketi v-safe; međutim, podnositelji registracije koji ukazuju na to da je nakon cijepljenja zatražena liječnička pomoć kontaktiraju osoblje VAERS -a i potiču ih da ispune VAERS izvješće.
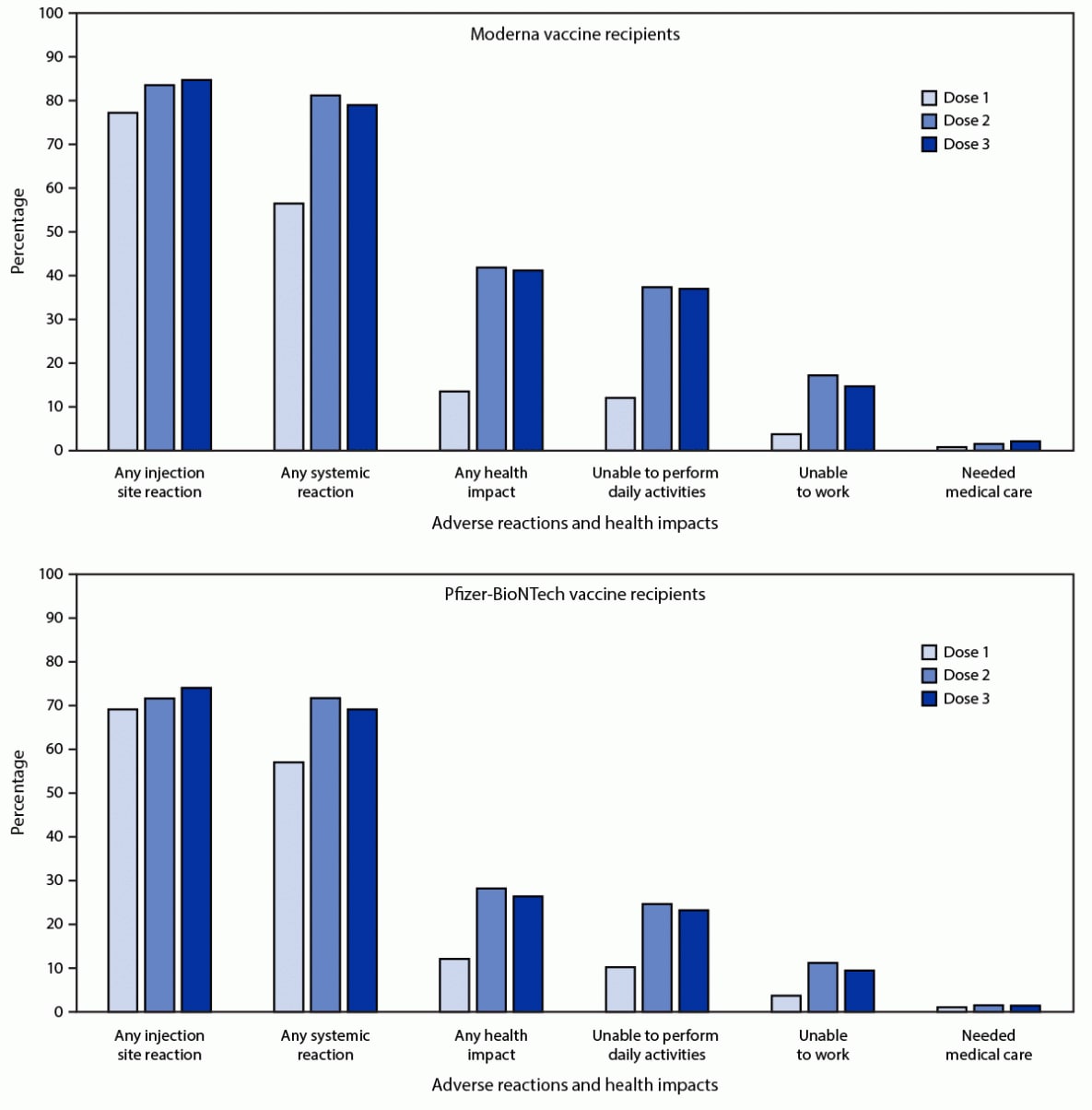
Među 21,658 v-sigurnih podnositelja registracije koji su primili isto cjepivo protiv mRNA za sve 3 doze, 12,591 (58.1%) je završilo barem jednu anketu o zdravstvenom pregledu dana 0–7 nakon sve 3 doze; 79.4% odnosno 74.1% prijavilo je lokalne ili sustavne reakcije, nakon doze 3, u usporedbi sa 77.6% i 76.5% koje su prijavile lokalne ili sustavne reakcije, nakon doze 2. Među podnositeljima registracije koje su primile 3 doze Moderne (6,283), lokalne reakcije su zabilježene češće nakon doze 3 nego doze 2 (5,323; 84.7% i 5,249; 83.5%; p-vrijednost = 0.03) (Lik). Sistemske reakcije zabilježene su rjeđe nakon doze 3 nego doze 2 (4,963; 79.0% i 5,105; 81.3%; p-vrijednost <0.001).
Među podnositeljima registracije koji su primili 3 doze Pfizer-BioNTech-a (6,308), lokalne reakcije su prijavljene češće nakon doze 3 nego doze 2 (4,674; 74.1% i 4,523; 71.7%; p-vrijednost <0.001). Sistemske reakcije zabilježene su rjeđe nakon doze 3 nego doze 2 (4,363; 69.2% i 4,524; 71.7%; p-vrijednost <0.001). Među onima koji su prijavili bol nakon doze 3 mRNA cjepiva, većina reakcija bila je blaga (4,909; 51.4%) ili umjerena (4,000; 41.9%); tešku bol (definiranu kao bol koja otežava ili onemogućava dnevne aktivnosti) prijavilo je 637 (6.7%).
Rasprava
Od 19. rujna 2021. godine približno 2.21 milijuna ljudi u Sjedinjenim Državama primilo je dodatne doze cjepiva protiv COVID-19†† nakon završetka primarne serije. Od 12. kolovoza do 19. rujna 2021. nisu primijećeni neočekivani obrasci nuspojava među 22,191 v-sigurnih podnositelja registracije koji su primili dodatnu dozu cjepiva protiv COVID-19. Većina prijavljenih lokalnih i sustavnih reakcija bile su blage do umjerene, prolazne i najčešće zabilježene dan nakon cijepljenja. Većina podnositelja registracije koji su primili dodatnu dozu prijavili su primarnu seriju cijepljenja protiv mRNA, nakon koje je uslijedila treća doza istog proizvođača.
Kliničko ispitivanje Pfizer-BioNTech, koje je obuhvatilo 306 osoba u dobi od 18 do 55 godina, pokazalo je da su reakcije nakon doze 3 usporedive s onima prijavljenim nakon doze 2 (3). Međutim, ovom analizom v-safe podataka utvrđeno je da su lokalne reakcije bile nešto češće, a sistemske reakcije rjeđe nakon doze 3 Pfizer-BioNTecha.
Obrasci nuspojava uočeni nakon doze 3 cjepiva Moderna ili Pfizer-BioNTech bili su u skladu s prethodno opisanim reakcijama nakon primitka doze 2
Broj podnositelja registracije koji su naveli da su primili 2 doze Janssenovog cjepiva ili su primili dodatnu dozu od proizvođača različitog od onog u njihovoj primarnoj seriji bio je mali, ograničavajući bilo kakve zaključke.
Podaci o sigurnosti ili učinkovitosti cijepljenja proizvodima cjepiva protiv COVID-19 različitih proizvođača su ograničeni; Savjetodavni odbor za imunizacijsku praksu (ACIP) preporučuje da osobe s umjereno do izrazito imunokompromitirajućim stanjima dobiju treću dozu cjepiva protiv mRNA COVID-19 od istog proizvođača kao i njihova primarna serija.
Preporuke CDC -a za dodatnu dozu trenutno ne uključuju osobe koje su primile cjepivo Janssen.
Tijekom razdoblja obuhvaćenog ovom studijom, preporuke ACIP-a za dodatnu dozu cjepiva protiv COVID-19 bile su ograničene na osobe s umjereno do izrazito imunokompromitirajućim stanjima koje su primile
2 doze cjepiva protiv mRNA.
Studija provedena među imunokompromitiranim pacijentima na hemodijalizi izvijestila je da su lokalne i sustavne reakcije nakon doze 3 cjepiva Pfizer-BioNTech slične onima nakon doze 2.¶¶ Nedavna izvješća o infekcijama kod cijepljenih osoba i porastu prevalencije infekcije varijantom B.1.617.2 (Delta) SARS-CoV-2, virusom koji uzrokuje COVID-19, među cijepljenim osobama možda su neke osobe potaknule da traže dodatnu dozu izvan preporuka. Medijan intervala od završetka primarne serije do primanja dodatne doze bio je približno 6 mjeseci; stoga su osobe s prioritetom tijekom uvođenja cjepiva protiv COVID-19, uključujući zdravstvene radnike i starije odrasle osobe, možda primile dodatnu dozu.
Nalazi u ovom izvješću podliježu najmanje četiri ograničenja. Prvo, upis u v-safe je dobrovoljan i vjerojatno nije reprezentativan za cijepljeno stanovništvo SAD-a; većina sudionika identificirala se kao bijelci i ne-latinoamerikanci. Drugo, tijekom ovog razdoblja ispitivanja dodatne preporuke za doze bile su ograničene na osobe s imunokompromitirajućim stanjima koje su završile primarnu seriju cijepljenja protiv mRNA COVID-19; međutim, v-safe ne uključuje podatke o imunološkom statusu.
Primatelji dodatne doze vjerojatno uključuju osobe sa i bez imunokompromitirajućih stanja. Treće, uzročno-posljedična veza između cjepiva i klinički ozbiljnih nuspojava prijavljenih nakon cijepljenja ne može se utvrditi upotrebom v-sigurnih podataka. Konačno, nisu bili dostupni dovoljni podaci za utvrđivanje obrazaca nuspojava nakon primitka dodatne doze od proizvođača koji je drugačiji od primarne serije ili za cjepivo Janssen.
Dodatna doza cjepiva protiv mRNA COVID-19 preporučuje se osobama s umjerenim do izrazito imunološkim poremećajima (5).
CDC je preporučio dodatnu dozu cjepiva Pfizer-BioNTech ≥ 6 mjeseci nakon završetka serije primarnih cjepiva među osobama starijim od 65 godina, stanovnicima u ustanovama za dugotrajnu skrb i osobama u dobi od 50 do 64 godine s podložnim medicinskim stanjima; osobe u dobi od 18 do 49 godina s osnovnim zdravstvenim stanjima i osobe u dobi od 18 do 64 godine s povećanim rizikom od izloženosti i prijenosa COVID-19 zbog profesionalnog ili institucionalnog okruženja mogu primiti dodatnu dozu na temelju svojih individualnih koristi i rizika
Početne analize podataka o sigurnosti od> 22,000 v-sigurnih podnositelja registracije pokazuju da su lokalne reakcije blago povećane, a sistemske reakcije blago smanjene nakon doze 3 mRNA nego nakon doze 2.
Nisu identificirani neočekivani obrasci nuspojava; prijavljeni su bili blagi do umjereni i prolazni. CDC će nastaviti pratiti sigurnost dodatnih doza cjepiva protiv COVID-19. Dodatni podaci o nuspojavama povezanim s različitim kombinacijama cjepiva i vremenu od završetka primarne serije bit će važni za usmjeravanje javnozdravstvenih preporuka.
| svojstvo | Moderna, %† (n = 10,601) | Pfizer-BioNTech, %† (n = 11,412) | Janssen, %†, § (n = 178) | ukupno (N = 22,191) | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Doza 3 Moderna (n = 10,453; 98.6%) | Doza 3 Pfizer-BioNTech (n = 144; 1.4%) | Doza 3 Janssen (n = 4; 0.04%) | Doza 3 Pfizer-BioNTech (n = 11,209; 98.2%) | Doza 3 Moderna (n = 197; 1.7%) | Doza 3 Janssen (n = 6; 0.1%) | Doza 2 Janssen (n = 48; 27.0%) | Doza 2 Moderna (n = 64; 36.0%) | Doza 2 Pfizer-BioNTech (n = 66; 37.1%) | ||
| Seks | ||||||||||
| ženski | 63.8 | 63.9 | 50.0 | 63.0 | 63.5 | 33.3 | 39.6 | 57.8 | 59.1 | 63.3 |
| Muški | 35.1 | 34.0 | 50.0 | 36.1 | 36.0 | 66.7 | 60.4 | 42.2 | 40.9 | 35.7 |
| nepoznat | 1.0 | 2.1 | 0 | 0.9 | 0.5 | 0 | 0 | 0 | 0 | 1.0 |
| Dobna skupina, god | ||||||||||
| 0-17 | 0.0 | 0.7 | 0.0 | 0.6 | 0.0 | 0.0 | 0.0 | 0.0 | 0.0 | 0.3 |
| 18-49 | 25.7 | 36.1 | 25.0 | 31.5 | 42.6 | 50.0 | 54.2 | 60.9 | 57.6 | 29.1 |
| 50-64 | 28.4 | 27.1 | 50.0 | 31.1 | 29.9 | 0.0 | 33.3 | 34.3 | 30.3 | 29.8 |
| 65-74 | 33.9 | 27.1 | 0.0 | 27.8 | 21.3 | 50.0 | 10.4 | 4.7 | 9.1 | 30.5 |
| 75-84 | 10.9 | 9.0 | 25.0 | 8.3 | 5.6 | 0.0 | 2.1 | 0.0 | 3.0 | 9.5 |
| ≥ 85 | 1.1 | 0.0 | 0.0 | 0.7 | 0.5 | 0.0 | 0.0 | 0.0 | 0.0 | 0.9 |
| Etnička pripadnost | ||||||||||
| Latino / Latino | 8.0 | 15.3 | 0 | 8.2 | 5.6 | 0 | 25.0 | 6.3 | 10.6 | 8.2 |
| Ne hispano/latino | 87.7 | 81.9 | 100 | 87.6 | 90.9 | 100 | 54.2 | 89.1 | 89.4 | 87.6 |
| nepoznat | 4.3 | 2.8 | 0 | 4.2 | 3.6 | 0 | 20.8 | 4.7 | 0 | 4.2 |
| Utrka | ||||||||||
| AI/AN | 0.5 | 0.7 | 0 | 0.5 | 0.5 | 0 | 2.1 | 0 | 0 | 0.5 |
| Azijski | 4.9 | 5.6 | 0 | 6.1 | 7.1 | 0 | 2.1 | 14.1 | 13.6 | 5.6 |
| Crna | 5.6 | 3.5 | 0 | 6.2 | 1.5 | 16.7 | 6.3 | 6.3 | 9.1 | 5.9 |
| NHPI | 0.2 | 0 | 0 | 0.3 | 0.5 | 0 | 4.2 | 0 | 0 | 0.3 |
| bijela | 82.6 | 82.6 | 100 | 80.4 | 85.8 | 66.7 | 56.3 | 71.9 | 69.7 | 81.4 |
| Rasno mješovit | 1.9 | 2.1 | 0 | 1.8 | 1.5 | 16.7 | 4.2 | 4.7 | 3.0 | 1.9 |
| drugo | 2.1 | 4.2 | 0 | 2.1 | 0.5 | 0 | 6.3 | 1.6 | 3.0 | 2.1 |
| nepoznat | 2.3 | 1.4 | 0 | 2.5 | 2.5 | 0 | 18.8 | 1.6 | 1.5 | 2.4 |
kratice: AI/AN = domoroci američkih Indijanaca/Aljaske; NHPI = domorodački Havajčanin ili drugi pacifički otočanin.
* Postotak podnositelja registracije koji su ispunili barem jednu anketu o sigurnom zdravstvenom pregledu u danima 0–7 nakon cijepljenja.
† Serija primarnih cijepljenja.
§ Uključuje osobe koje su primile primarnu Janssenovu jednokratnu dozu i 1 dodatnu dozu cjepiva od navedenih proizvođača.
| Reakcija | Moderna, %† (n = 10,477) | Pfizer-BioNTech, %† (n = 11,284) | Janssen, %†, § (n = 174) | ukupno (N = 22,191) | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Doza 3 Moderna (n = 10,453; 98.6%) | Doza 3 Pfizer-BioNTech (n = 144; 1.4%) | Doza 3 Janssen (n = 4; 0.04%) | Doza 3 Pfizer-BioNTech (n = 11,209; 98.2%) | Doza 3 Moderna (n = 197; 1.7%) | Doza 3 Janssen (n = 6; 0.1%) | Doza 2 Janssen (n = 48; 27.0%) | Doza 2 Moderna (n = 64; 36.0%) | Doza 2 Pfizer-BioNTech (n = 66; 37.1%) | ||
| Dani od primarne serije, medijan (IQR) | 182 (164 - 198) | 183 (161 - 204) | 173 (141 - 182) | 183 (157 - 209) | 186 (161 - 217) | 123 (113 - 182) | 84 (16 - 136) | 156 (140 - 164) | 150 (136 - 167) | 182 (160 - 202) |
| Bilo koja reakcija na mjestu ubrizgavanja | 80.9 | 64.6 | 75.0 | 69.4 | 81.7 | 83.3 | 25.0 | 70.3 | 80.3 | 74.9 |
| Svrabež | 20.0 | 11.8 | 0 | 8.4 | 10.2 | 16.7 | 10.4 | 6.3 | 7.6 | 13.9 |
| Bol | 75.9 | 60.4 | 75.0 | 66.6 | 80.2 | 83.3 | 20.8 | 68.8 | 74.2 | 71.0 |
| Crvenilo | 25.2 | 8.3 | 0 | 9.8 | 20.8 | 16.7 | 6.3 | 7.8 | 12.1 | 17.1 |
| Oteklina | 33.6 | 17.4 | 0 | 16.8 | 30.5 | 16.7 | 6.3 | 12.5 | 18.2 | 24.8 |
| Svaka sustavna reakcija | 75.2 | 59.7 | 50.0 | 65.1 | 76.1 | 100 | 31.3 | 68.8 | 63.6 | 69.9 |
| Bol u trbuhu | 8.4 | 3.5 | 0 | 6.4 | 8.1 | 16.7 | 4.2 | 3.1 | 6.1 | 7.3 |
| Mialgija | 49.8 | 29.2 | 0 | 36.3 | 49.2 | 50.0 | 20.8 | 45.3 | 33.3 | 42.7 |
| Zimica | 31.3 | 8.3 | 50.0 | 17.5 | 33.5 | 50.0 | 8.3 | 23.4 | 10.6 | 24.1 |
| Proljev | 9.9 | 7.6 | 0 | 9.0 | 9.6 | 16.7 | 8.3 | 6.3 | 9.1 | 9.4 |
| Umor | 61.8 | 44.4 | 0 | 51.0 | 60.9 | 83.3 | 14.6 | 48.4 | 50.0 | 56.0 |
| Groznica | 36.4 | 20.1 | 50.0 | 22.2 | 37.1 | 50.0 | 6.3 | 37.5 | 12.1 | 29.0 |
| Glavobolja | 49.0 | 31.1 | 0 | 38.4 | 49.7 | 83.3 | 18.8 | 35.9 | 40.9 | 43.4 |
| Bol u zglobovima | 33.0 | 18.8 | 0 | 23.0 | 31.0 | 33.3 | 16.7 | 20.3 | 19.7 | 27.7 |
| Mučnina | 18.8 | 10.4 | 25.0 | 13.6 | 21.3 | 33.3 | 8.3 | 9.4 | 18.2 | 16.1 |
| Osip | 2.3 | 0.7 | 0 | 1.9 | 2.5 | 0 | 4.2 | 1.6 | 1.5 | 2.1 |
| Povraćanje | 2.2 | 2.1 | 25.0 | 1.4 | 2.0 | 0 | 2.1 | 0 | 0 | 1.7 |
| Svaki utjecaj na zdravlje | 39.2 | 19.4 | 0 | 25.2 | 39.1 | 33.3 | 16.7 | 28.1 | 24.2 | 31.8 |
| Ne može obavljati uobičajene dnevne aktivnosti | 35.2 | 18.1 | 0 | 22.1 | 33.0 | 33.3 | 10.4 | 25.0 | 15.2 | 28.3 |
| Ne mogu raditi ili pohađati školu | 13.7 | 4.9 | 0 | 9.0 | 21.3 | 16.7 | 10.4 | 6.3 | 13.6 | 11.3 |
| Potrebna medicinska njega | 2.1 | 1.4 | 0 | 1.5 | 3.0 | 0 | 6.3 | 0 | 0 | 1.8 |
| Telehealth | 0.9 | 0.7 | 0 | 0.7 | 1.0 | 0 | 2.1 | 0 | 0 | 0.8 |
| Klinika | 0.7 | 0.7 | 0 | 0.6 | 0.5 | 0 | 4.2 | 0 | 0 | 0.6 |
| Hitni posjet | 0.2 | 0 | 0 | 0.2 | 0 | 0 | 4.2 | 0 | 0 | 0.2 |
| Hospitalizacija | 0.05 | 0 | 0 | 0.1 | 0 | 0 | 0 | 0 | 0 | 0.1 |
LIK. Nuspojave i utjecaji na zdravlje koje su prijavile osobe koje su primile 3 doze* cjepiva Moderna (N = 6,283) ili Pfizer-BioNTech (N = 6,308) protiv COVID-19 i završile najmanje jedno ispitivanje v-safe check-in dana u danima 0– 7 nakon svake doze, prema broju doza - Sjedinjene Države, 12. kolovoza - 19. rujna 2021